不同微生物宿主中通用基因回路的功能可预测性
过去 20 年里,合成生物学家一直在尝试在活细胞中构建生物回路,以实现特定的行为,如布尔逻辑门、信号滤波器、振荡器、状态机、传感器和基因控制器。这些电路是通过将基因“部件”与某些交换逻辑连接起来,自下而上地从头构建起来的。然而,这些成就主要局限于大肠杆菌 和酿酒酵母等少数模式生物。由于宿主特异性的基因表达机制、代谢和不同的 DNA 载体,将这些基因部分转移到非模式生物中具有挑战性。因此,开发能够在多种生物体中稳健且可预测地运行的通用基因回路至关重要。理想的通用基因回路应该与宿主环境(包括细胞外、细胞和遗传环境)隔离。
近日,北京大学欧阳谦实验室和中科院楼继伟实验室合作团队在《 定量生物学》杂志上发表了《不同微生物宿主中通用基因回路的功能可预测性》论文。该团队通过建立定量框架来探索非模式生物中生物部件的普适性和可靠性,在链霉菌、 谷氨酸棒杆菌、 恶臭假单胞菌和 大肠杆菌四种微生物宿主中表征了通用的遗传部件,即T7 RNA聚合酶激活模块和一组转录抑制模块。基于这些部件优异的普适性,严格证明了遗传回路的功能可预测性。
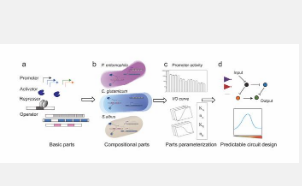
图1展示了跨物种遗传电路自下而上的设计流程。首先对来自细菌和噬菌体的转录调控元件进行标准化,并用单一反应模型对这些元件进行基准测试,以确保它们在宿主生物中表现一致。然后,对部件进行组合表征,并通过详细建模进行参数化。从测量中提取定义这些部件行为的关键参数,并将其归类为内在的或宿主特定的。最后,将标准化部件组合成复杂的电路,并使用组合建模和模拟来预测电路在不同宿主生物中的行为。浙江大学的王宝军教授在同一期的评论中写道:“这些发现为可预测地设计和调节具有复杂功能的通用遗传电路铺平了道路,……并为实现不同宿主中通用电路的设计自动化具有巨大的潜力。”
免责声明:本答案或内容为用户上传,不代表本网观点。其原创性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容、文字的真实性、完整性、及时性本站不作任何保证或承诺,请读者仅作参考,并请自行核实相关内容。 如遇侵权请及时联系本站删除。
