该研究由兰勋博士(清华大学医学院基础医学系,中国北京)、季家福博士、卜昭德博士(北京大学肿瘤医院暨肿瘤研究所胃肠肿瘤中心,中国北京)、余洪浩博士(桂林医科大学广西药物研发与优化重点实验室)、吴文明博士、赵玉沛博士、彭俊亚博士(北京协和医学院北京协和医院,中国北京)和崔培林博士(首都医科大学天坛医院,中国北京)领导。
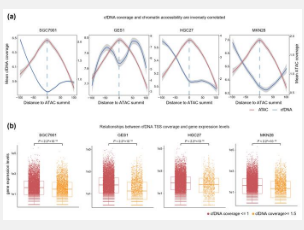
可以从循环游离DNA(cfDNA) 特征(例如启动子处的组蛋白修饰和碎片化模式)推断出肿瘤细胞基因表达模式。然而,cfDNA 特征与肿瘤特异性染色质可及性之间的直接相关性仍未最终确定,因此目前其应用主要局限于癌症诊断。在进行主动转录的基因中,启动子会经历核小体解离,从而降低其在 cfDNA 内的保存和可检测性。因此,启动子区域的 cfDNA 覆盖范围可以作为染色质景观的代理,反映活细胞内的基因表达水平。
体外细胞培养cfDNA模型发现,cfDNA转录起始位点(TSS)覆盖率低的基因与染色质可及性增加和表达水平升高相关。他们对四种细胞系(SGC7901、GES1、HGC27和MKN28)进行了ATAC-seq和RNA-seq分析。此外,还对细胞外培养基(DMEM)中的cfDNA进行了测序分析。研究表明,cfDNA的TSS覆盖率与基因的染色质可及性和转录水平呈负相关。“这个细胞系实验非常有趣,”Xun说。
此外,STAD 和 BRCA 患者血液样本中的 cfDNA TSS 覆盖率与 TCGA 数据集中相应肿瘤组织中的 ATAC-seq 覆盖率呈负相关。STAD 中的 Pearson 相关系数为 -0.65(P值 < 2.2×10 -16),BRCA 中的 Pearson 相关系数为 -0.55(P值 < 2.2×10 -16)。此外,肿瘤组织中 ATAC-seq 信号高的基因的 cfDNA TSS 覆盖率低于 cfDNA TSS 覆盖率低的基因( STAD 和 BRCA 的P值均 < 2.2×10 -16)。
TCGA STAD RNA-seq数据集中,与cfDNA TSS覆盖率低的基因相比,cfDNA TSS覆盖率高的基因表达水平明显降低(P值<2.2×10-16 )。低cfDNA TSS覆盖率的基因在多种癌症相关通路和生物学功能中富集,包括胃癌、细胞周期、MAPK信号通路、Wnt信号通路。接下来,他们从TCGA STAD RNA-seq数据和TCGA BRCA RNA-seq数据中计算了肿瘤和正常组织之间所有基因的差异表达模式。与体外细胞系的结果一致,TCGA STAD肿瘤样本和TCGA BRCA肿瘤样本中上调的基因的cfDNA TSS覆盖率明显低于下调的基因( cfDNA TSS覆盖率P值<2.2×10-16 )。
此外,该团队对来自 546 名个体的血浆 cfDNA 进行了详尽分析,这些个体包括患有 21 种不同疾病类型的患者以及健康捐赠者。他们发现,这种反比关系可以识别出患有癌症的患者。他们从一个广泛的群体中收集了外周血 cfDNA,包括胃癌患者 ( n =101)、乳腺癌患者 ( n =57)、胰腺癌患者 ( n =40)、胃炎患者 ( n =83)、非癌症疾病(如骨病、脑出血、心脏病、良性肿瘤等)患者 ( n =58) 和健康个体 ( n =100),以研究癌症特异性 cfDNA 特征。研究发现,启动子区域的cfDNA覆盖度可以准确区分健康个体中的胃癌(STAD,AUC 0.96)、乳腺癌(BRCA,AUC 0.98)和胰腺导管腺癌(PDAC,AUC 0.88),以及患有胃炎、非癌症疾病和其他类型癌症的患者。
他们进一步在独立队列中探索了这些癌症类型特异性基因的 cfDNA TSS 覆盖率。他们开发了一种靶向测序检测方法,称为 cfDNA 开放染色质捕获测序 (CFOCUS),利用杂交捕获 STAD 特异性基因,并在 80 个血浆样本队列中验证了其性能,其中包括 35 名胃癌患者和 45 名健康个体。这 35 名胃癌患者包括早期样本(I 期和 II 期),这增强了癌症筛查的稳健性。使用为 STAD 患者 cfDNA WGS 数据建立的相同模型,癌症风险比例大于 0.5 的 CFOCUS 样本被视为患有 STAD 的患者。CFOCUS 的 AUC 达到 0.88(80% 的敏感性和 91% 的特异性)。每位健康供体的三个重复 cfDNA 样本的平均 Pearson 系数分别为 0.93、0.88 和 0.90,这凸显了他们研究中使用的定制探针组的稳健性。这些结果证明了 cfDNA 覆盖特征在早期癌症检测中的潜在效用。
